Im neusten Beitrag von Dr. Andreas Thomas beschreibt er, inwiefern sich die Methoden des CGM (kontinuierliches Glukosemonitoring) unterscheiden.
Im letzten Beitrag wurde versprochen, auf verschiedene Anwendungsformen des CGM einzugehen.
Charakteristisch ist, dass CGM die Diabetologie in verschiedene Richtungen verändert bzw. sogar revolutioniert. Hervorzuheben ist dabei, dass CGM
- eine diagnostische Methode darstellt, welche einen lückenlosen Einblick in die dynamische Regulierung des Glukoseverlaufs bietet,
- den Patienten ein „Biofeedback“ liefert,
- grundlegend die Sicht auf den Glukosestoffwechsel und dessen Beurteilung ändert,
- nur minimal-invasiv und damit weniger belastend für die Patienten ist als die Blutglukosemessung, wodurch sich diese minimieren, zum Teil sogar ersetzen lässt,
- eine Methode zur Therapieunterstützung darstellt, besonders von insulinbehandelten Patienten (sensorunterstützte Therapie (ICT plus CGM), sensorunterstützte Pumpentherapie (CSII plus CGM)), aber auch darüber hinaus,
- gerätetechnisch ein Teil von AID-Systemen (AID – automated insulin delivery; automatisierte Insulindosierung) ist und eine grundlegende Voraussetzung dafür darstellt,
- unter der Voraussetzung vorliegender Interoperabilität die Möglichkeit der Kopplung mit verschiedenen Geräten (Smart-Pens, Insulinpumpen bis hin zu AID-Systemen) und Softwarelösungen bietet,
- ein wichtiges Instrument zur Digitalisierung darstellt (Übergabe und Analyse der Daten in Datenmanagementsystemen, Patienten- und Therapieentscheidungshilfssystemen).
Diese Anwendungsbreite macht CGM zu einer der wichtigsten, vielleicht sogar der wichtigsten Innovation für die Diabetologie der letzten Jahrzehnte.
Bei seiner ersten Zulassung im Jahr 1999 war CGM ausschließlich ein diagnostisches Werkzeug. Das damalige CGMS®Gold (Medtronic) war ein verblindetes System. Das heißt, die Glukosewerte wurden nicht unmittelbar angezeigt, waren also auch nicht nutzbar für die Unterstützung der Therapie. Erst nach der Messung über 3 Tage erfolgte der Download der Daten in eine spezielle Software und nach deren Analyse die Darstellung der Glukoseprofile und der statistischen Parameter. Man bezeichnete dieses System auch als „Holder“, in Anlehnung an ein 24-Stunden-EKG oder 24-Stunden-Blutdruckmessgerät. Dieses CGM lag ausschließlich im Nutzungsbereich der Ärzte.
Die Patienten wünschten sich dagegen ein CGM für die Anwendung unter Alltagsbedingungen, also zur Unterstützung ihrer Diabetestherapie. Das setzt voraus, dass die aktuellen Glukosewerte auf dem Display eines Monitors, einer Insulinpumpe oder eines Smartphones dargestellt werden. Grundsätzlich können alle aktuell verwendeten CGM-Systeme die Glukosedaten anzeigen, die sich natürlich auch zu Diagnosezwecken von dem medizinische Personal nutzen lassen. Dabei ist zu berücksichtigen, dass der Glukoseverlauf nicht allein die Regulierung des Stoffwechsels durch die Therapie zeigt, sondern auch durch den Patienten beeinflusst wird, wenn er diesen beobachten kann.
Zwei Anwendungsfelder des CGM im Alltag
Herausgebildet haben sich zwei Anwendungsfelder des unter Alltagsbedingungen nutzbaren CGM: das rtCGM (Real-Time-CGM) und das iscCGM (CGM mit intermittierendem Scannen). Dabei ist es zunächst egal, ob die Glukosewerte sofort sichtbar sind (rtCGM) oder ob dazu vorher noch eine Handlung auszuführen ist, wie das Scannen des Glukosesensors mit dem Monitor oder dem Smartphone (iscCGM). In beiden Fällen handelt es sich technisch um ein Real-Time-CGM, seitens der therapeutischen Anwendung liegt der Unterschied jedoch in der Notwendigkeit des Scannens, also darin, eine Handlung ausführen zu müssen, bevor die Daten einsehbar sind. Letzteres betrifft die Geräte FreeStyle Libre der ersten Generation (ohne Alarmierungsmöglichkeit) und FreeStyle Libre 2 (mit optional einstellbaren Alarmen) des Unternehmens Abbott.
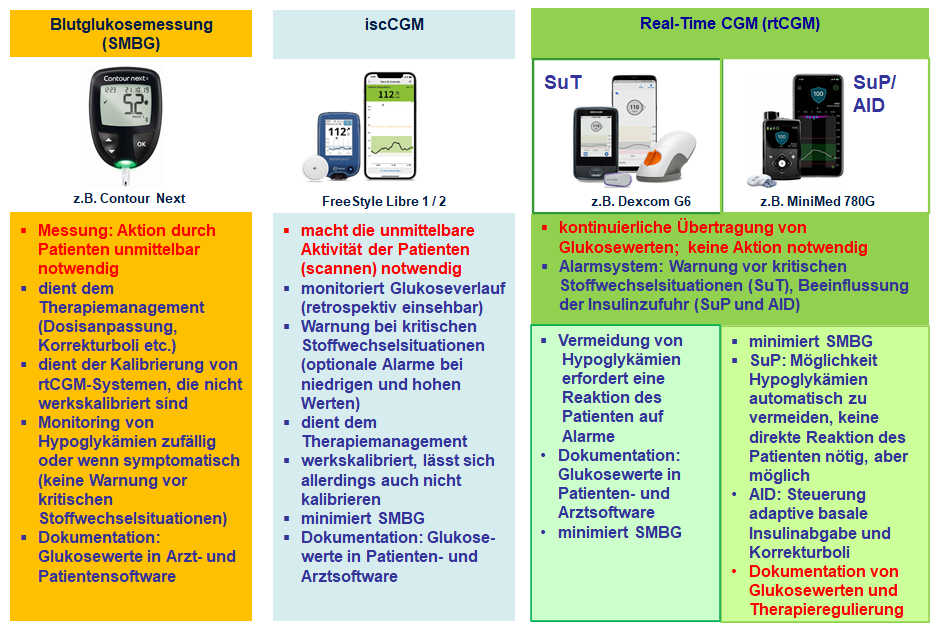
Im Prinzip ordnet sich das iscCGM methodisch ein zwischen der Blutglukosemessung (SMBG – self measurement of blood glucose; Selbstmessung der Blutglukose) und dem rtCGM mit den sich daraus ergebenden Möglichkeiten, über das Glukosemanagement hinaus auch ein Insulinmanagement zu realisieren (Abb. 1). Aktuell sind die beiden iscCGM-Geräte die weltweit am meisten genutzten Systeme (ca. 4 Millionen Anwender weltweit) [1], wobei deren wichtigstes Anwendungsgebiet in der Minimierung des SMBG zu sehen ist. Dazu trägt bei, dass die FreeStyle-Libre-Sensoren werkskalibriert sind und sich auch gar nicht kalibriere lassen. Der Patient nutzt SMBG also nur noch, wenn er die angezeigten Werte einmal überprüfen will.
Die Zahl der Anwender eines rtCGM ist geringer als beim iscCGM. Weltweit nutzen dies etwa 1 Millionen Patienten, davon circa 650.000 mit einem AID-System. Gegenüber dem iscCGM liegt beim rtCGM eine Differenzierung vor. Im einfachsten Fall wird ein rtCGM zusätzlich und unabhängig von der bestehenden Therapieform genutzt. Bei der sensorunterstützten Therapie (SuT) betrifft das in der Regel die intensivierte Insulintherapie (ICT).
Das rtCGM kann den Anwender vor zu hohen und zu tiefen Glukosewerten warnen, zum Beispiel über eingestellte Voralarme und natürlich durch Blick auf die fortlaufend angezeigte Glukosekurve. Daraus kann er vorausschauend reagieren, die Entwicklung des Glukoseverlaufs beobachten, zum Beispiel nach einer Mahlzeit oder beim Sport. Gleiches betrifft die Kombination mit der Insulinpumpentherapie (CSII), woraus sich die sensorunterstützte Pumpentherapie (SuP) ergibt.
In der Regel ist das CGM dabei aber nicht mehr unabhängig von der Insulinpumpe und sendet die Glukosedaten auf deren Display. Seit 2009 wurde die SuP schrittweise modifiziert, indem der Glukosesensor zunehmend auch auf die Insulinabgabe Einfluss nahm. So erfolgte zunächst die Unterbrechung der Insulinzufuhr, wenn die Glukosewerte den eingestellten Wert für eine Hypoglykämieschwelle erreichten. Später wurde das Hypoglykämienmanagement eingeführt.

Bei sinkenden Glukosewerten und der Gefahr einer Hypoglykämie in der nächsten Zeit (bei der MiniMed 640G waren das 30 Minuten) unterbrach die Insulinpumpe die Insulinabgabe (also bereits, bevor sich eine Unterzuckerung einstellte) und schaltete diese wieder zu, wenn die Gefahr vorbei war. Seit 2016 (in Deutschland seit 2019) wird die Insulinabgabe zum Teil vom CGM gesteuert. Bei dem ersten Gerät dieser Art, der MiniMed 670G, und bei allen nachfolgenden Systemen MiniMed 780G, t:slim X2 CONTROL IQ, Accu-Chek Insight mit Diabeloop wird die basale Insulinabgabe adaptiv gesteuert. Das heißt, die aktuell von dem rtCGM gemessenen Glukosewerte werden mit Hilfe eines Algorithmus so verarbeitet, dass ein gewählter Glukosezielwert erreicht wird.
Die Boli zur Mahlzeit werden dagegen bei diesen Hybrid-AID-Systemen weiterhin manuell abgegeben (deswegen „Hybrid“: automatische basale Insulingabe, manueller Bolus). Dagegen werden die Korrekturboli bei den letzten drei genannten Systemen ebenfalls automatisch dosiert. Es ist einleuchtend, dass das Zusammenwirken des rtCGM mit verschiedenen Ebenen des Insulinmanagements zu völlig unterschiedlichen Therapiemodifikationen führt und damit auch zu einer unterschiedlichen Qualität der Diabeteseinstellung.
Es sind noch zwei weitere Optionen für die Anwendung des rtCGM gegeben. Die eine betrifft das Zusammenwirken mit Smart-Pens. Über eine Bluetooth-Verbindung wirkt der Smart-Pen mit dem CGM zusammen. Weiterhin ist das System mit einer Smartphone-App verbunden. Der Anwender kann so die Wirkung der gegebenen Insulinboli verfolgen, das verbleibende Insulin berechnen lassen und Dosierungserinnerungen erhalten. Das kann unter anderem zu einer digitalen Gesundheitsanwendung (DiGA) führen, welche, wenn zugelassen, von dem Arzt per Rezept verordnet werden kann. Schließlich lassen sich die CGM-Daten nutzen, um von einem zentralen Computer aus Handlungsempfehlungen auf das Smartphone des Anwenders zu schicken. Derzeit sind solche PDSS (patient decision support systems; Patientenentscheidungshilfssysteme) in Deutschland noch nicht zugelassen.
Die gesamte genannte Palette von therapeutischen Optionen mit Hilfe von rtCGM-Systemen erfordert Interoperabilität. Daraus folgt, dass sich das Glukosemanagement mit dem Insulin-, Daten- und Alltagsmanagement vereinigt. Deshalb wurde ein sogenanntes iCGM durch die amerikanische Food and Drug Administration (FDA) definiert, was integriertes, interoperables CGM bedeutet. Als Erstes erfüllte das rtCGM Dexcom G6 von Dexcom dieses Prädikat. Der Guardian 4 von Medtronic und der FreeStyle Libre 3 werden diesem folgen. Neben der prinzipiellen Möglichkeit der Kopplung des rtCGM-Systems an verschiedene Geräte und Softwarelösungen wird dabei auch eine entsprechend hohe Anforderung an die Messqualität definiert [2]. Darauf werde ich demnächst eingehen.
[1] Kelly Close Report. Diabetes Technology 3Q21 Industry Roundup 19.01.2022
[2] American Food and Drug Administration. Integrated continuous glucose monitoring system. DEN170088, March 27, 2018.
Zum ersten Teil der Reihe von Dr. Andreas Thomas um das CGM im Diabetes-Management gelangt ihr hier: Systeme für das kontinuierliche Glukosemonitoring (CGM): methodisch-technischer Überblick.


Sehr informativ. Ich nutze FreeStyleLibre 2 und bin sehr zufrieden. Der Umstieg auf Libre 3 ist schief gegangen. Die Sensoren meldeten laufend falsche, zu niedrige Werte. Gibt es ähnliche Fälle?